Importancia de la monitorización hemodinámica en el aporte de oxígeno a los ejidos
El aporte de oxígeno (O2) a los tejidos sólo es posible si se mantiene una adecuada circulación sanguínea. La demanda de oxígeno es la que conduce al sistema cardiovascular a realizar los ajustes necesarios en respuesta a la misma.
Un sistema cardiovascular sano, mantiene este aporte de O2 a los tejidos bajo cualquier situación metabólica, que se modula de forma dinámica a cuatro niveles:
- Volumen intravascular
- Inotropismo
- Vasoactividad
- Cronotropismo
Las tres primeras son mecanismos que generan cambios en la presión arterial (presión arterial media PAM) y en el flujo sanguíneo (volumen sistólico VS) mientras que el último modula el flujo de perfusión.
Así, el organismo actuará en estos cuatro niveles con el objetivo de ajustar el estado hemodinámico, sin olvidar el papel que la demanda de O2 tiene en los cambios que se producen en estos moduladores.
El tratamiento clínico de cualquier alteración hemodinámica puede afectar sólo a nivel de estos cuatro moduladores, pero no afectará de manera directa a las consecuencias de ese efecto modulador.
En el paciente inestable, la exploración física suele ser insuficiente para determinar el estado patológico y seleccionar la mejor terapia.
Por tanto, en estos casos se recomienda la monitorización hemodinámica. Esta permite determinar de forma clara y precisa el tipo de alteración y aplicar el tratamiento más adecuado, pudiendo además evaluar la respuesta del paciente a dichas terapias.
Durante las últimas décadas, las técnicas de monitorización hemodinámica han evolucionado de intermitentes a mediciones continuas y a tiempo real y desde invasivas hacia métodos menos invasivos incluso no invasivos, con la incorporación de un gran número de variables y la capacidad de proporcionar gran cantidad de información sobre esas variables hemodinámicas.
A día de hoy sin embargo, sigue existiendo un debate en cuanto al grado de invasividad y de frecuencia en el seguimiento, necesarios para definir el beneficio aunque la mayor invasividad proporciona una visión más estable y pluripotencial que puede permitir una mejor titulación de la atención en los pacientes más críticos.
Que es la monitorización hemodinámica
La monitorización hemodinámica consiste en las técnicas capaces de evaluar el estado hemodinámico de los pacientes y su objetivo es mantener una adecuada perfusión tisular. De hecho, si los órganos vitales están hipoperfundidos, los pacientes críticamente enfermos pueden desarrollar una disfunción de diferentes sistemas orgánicos.
La aparición y mantenimiento de este síndrome de disfunción multiorgánica parece estar relacionado con alteraciones hemodinámicas sistémicas y la perfusión orgánica. Estas condiciones afectan la microcirculación a nivel de los tejidos, resultando en hipoxia tisular.
El tiempo es crucial en el diagnóstico de las alteraciones hemodinámicas porque su tratamiento precoz parece mejorar los resultados en estas situaciones. Para ello, la monitorización hemodinámica debe ser efectiva y capaz de lograr los objetivos que estén asociados a una mejora de los resultados.
Justificación de la monitorización hemodinámica
Las nuevas tecnologías recientemente desarrolladas, nos brindan la posibilidad de comprender el mecanismo de descompensación del paciente y nos guían hacia intervenciones terapéuticas adecuadas.
La monitorización hemodinámica permite tener controles históricos, comprender la fisiopatología del proceso y corregir los trastornos de base. Nos proporciona la información sobre cómo definir y tratar los diferentes patrones fisiopatológicos que se puede conseguir mediante técnicas invasivas o no invasivas, continuas o intermitentes.
Sin embargo, no existe dispositivo de monitorización hemodinámica que mejore los resultados a menos que esté asociado a un tratamiento adecuado y eficaz.
Los datos clínicos sugieren que la reanimación excesiva con líquidos empeora los resultados. Por tanto, el uso de variables dinámicas que permitan evaluar la capacidad del paciente de responder a los fluidos durante la reanimación nos ayuda a limitar la infusión en pacientes que no responden.
Del mismo modo sucede con el tratamiento inotrópico, donde se puede administrar estos fármacos para conseguir el mayor beneficio con la menor dosis posible cuando se titula con objetivos hemodinámicos.
Y así queda definida la justificación de la monitorización hemodinámica a tres niveles.
- Un primer nivel para identificar estados patológicos no específicos, de nueva aparición en pacientes de riesgo.
- Un segundo nivel para definir enfermedades cardiovasculares específicas del paciente, conocer su estado cardiovascular para personalizar y optimizar la reanimación.
- Un tercer nivel donde la monitorización hemodinámica permite identificar de forma precoz la descompensación clínicamente relevante.
En su nivel más alto, la monitorización hemodinámica pretende demostrar la mejora de los resultados obtenidos con un uso más efectivo de las terapias y tras identificar los estados patológicos que nos permitan un tratamiento dirigido.
De esta manera se minimizan los efectos iatrogénicos al limitar esas terapias en los pacientes que tienen menos probabilidades de beneficiarse de su uso.
Los resultados deben estar centrados en el paciente: disminución de la estancia en UCI y hospitalaria, menor duración del tiempo bajo ventilación mecánica, reducción de la lesión renal aguda y otras complicaciones agudas, inicio de la ingesta oral, etc.
Monitorización y variables hemodinámicas
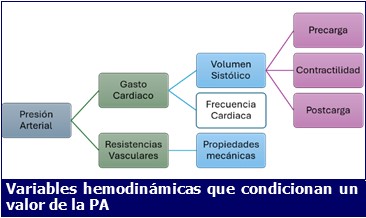
Presión arterial
La Presión arterial (PA) es quizá el parámetro hemodinámico medido con mayor frecuencia. Esta presión es la fuerza ejercida por la circulación de la sangre que impulsa la misma a través de los órganos y lo tejidos, es decir la perfusión sanguínea.
La perfusión tisular no se puede medir directamente en la práctica clínica ya que la perfusión de un órgano depende de la presión arterial – la presión venosa/resistencias. Esa presión de perfusión y las resistencias vasculares a nivel local son las que determinarán la perfusión del órgano.
Sin embargo, se considera a la presión arterial como una estimación de la perfusión tisular, pero esto solo sucede si la presión venosa y las resistencias son constantes.
En condiciones de estabilidad hemodinámica, las demandas metabólicas locales controlan el flujo y la perfusión del órgano se mantiene en un rango normal por la regulación el tono vascular local.
En condiciones patológicas este sistema de autorregulación se deteriora y el flujo depende de la presión de perfusión. Por tanto, medir la PA en concreto la PAM resulta una forma indirecta de medir la presión de perfusión.
Como la PA es el resultado de múltiples variables hemodinámicas, la aparición de hipotensión no siempre va a ser equivalente y dependerá del mecanismo fisiopatológico subyacente.
Es por tanto necesario conocer e identificar qué elementos del sistema cardiovascular están siendo los responsables de la inestabilidad.
Gasto cardiaco
El GC no es sólo un determinante de la presión arterial, sino que se asocia con la perfusión de los órganos de tal forma que cuando hay un descenso de la PA, la perfusión de los órganos puede mantenerse estable cuando el GC permanece estable.
Esto es fácilmente comprensible si vemos la perfusión de los órganos como un porcentaje del GC que se distribuye a todos los tejidos. Esta visión de la relación del GC con la perfusión tisular enriquece la visión tradicional sobre la perfusión de los órganos como la presión de perfusión dividida por las RVS.
De aquí se deriva la importancia de monitorizar y mantener el GC cuando el objetivo final es mantener la perfusión de los órganos. Sin embargo, esta visión no puede aplicarse a todas las condiciones patológicas como la sepsis o el shock donde existe una disfunción microcirculatoria y el desacoplamiento entre la macrocirculación y la microcirculación son características destacadas.
No hay que olvidar que los cambios en las demandas de oxígeno juegan un papel principal en la regulación del GC y es importante minimizar las demandas de O2 en los pacientes críticos (p.ej. ajustando la sedación).
Presión Venosa Central
La presión venosa central (PVC) sigue siendo una variable utilizada frecuentemente a la hora de administrar fluidos a pesar de los numerosos estudios que demuestran que no es un parámetro fiable para medir la respuesta a fluidos y la mayoría de las guías ya no recomiendan su uso para tal fin18. En este sentido, debemos de dejar de usar la PVC para estimar la precarga del paciente.
La PVC se ha utilizado como medida de precarga por la relación directamente proporcional entre presión y tensión y se considera precarga la tensión del miocardio al final de la diástole. Sin embargo, la PVC es una presión intracavitaria.
La precarga no se define solo por la presión intravascular sino también por la presión que rodea el corazón, siendo la presión pericárdica en condiciones normales casi idéntica a la PVC.
La presión transmural (PVC- P, pleural) se relaciona con la fuerza que distiende las cavidades cardiacas y es lo que realmente define la precarga cardiaca, razón por lo que la PVC debe medirse al final de la espiración. En situaciones patológicas esta presión transmural puede aumentar significativamente, lo que anula este enfoque.
Además, hay condiciones patológicas como la hiperinsuflación pulmonar o la hipertensión intraabdominal que producen un aumento de la presión pleural. Esta presión se transmite a las cavidades cardiacas, aumentando la PVC. Sin embargo, la presión transmural y la precarga cardiaca pueden reducirse.
Otro factor a considerar al utilizar la PVC para estimar la precarga es que el volumen telediastólico (VED) no se relaciona con la presión de manera lineal. La distensibilidad auricular disminuye a medida que aumenta el VED, con lo que aumenta la PVC a medida que lo hace este.
En situaciones patológicas como la isquemia miocárdica o el shock séptico esta relación está habitualmente alterada existiendo un mismo valor de PVC para diferentes valores de VED.
Finalmente, la PVC resulta de la interacción entre la función del ventrículo derecho y el retorno venoso y en consecuencia un mismo valor de PVC puede representar diferentes estados de función ventricular y de retorno venoso.
Pero además de su valor limitado como índice de precarga, la PVC tampoco puede predecir si el GC aumentará después de la administración de fluidos. Esto se debe a que el GC no depende solo de los cambios de la precarga sino también de la función ventricular.
Futuro de la monitorización hemodinámica
En el ámbito de la salud digital, los dispositivos del futuro deben combinar las siguientes características: ser no invasivos, ergonómicos y fáciles de usar. Además, deben ser inalámbricos o portátiles, e integrar software inteligente y algoritmos.
En cuanto a las diferentes técnicas de monitorización, es necesario mejorar la fiabilidad que permita a los clínicos monitorizar la PA de forma no invasiva. La futura monitorización hemodinámica debería integrar también el seguimiento de la perfusión regional y la microcirculación.
Las alteraciones en la microcirculación y la disociación entre micro y macrocirculación, ocurre en pacientes con shock sobre todo de origen séptico.
Por lo tanto, monitorizar la microcirculación podría ser de interés para comprender mejor los mecanismos que causan el shock y para seleccionar y ajustar mejor las terapias.
Esto garantizaría que una mejora de la macrocirculación realmente resulta en la mejora de la microcirculación, según el principio de coherencia hemodinámica.
Actualmente, el único lecho microcirculatorio que podemos investigar a pie de cama es el de la microcirculación sublingual, gracias a un dispositivo portátil de microcopia. Sin embargo, el análisis de la microcirculación a día de hoy tiene dos importantes limitaciones.
La primera es que la alteración de la microcirculación sublingual durante el shock puede no ser completamente representativa de otros territorios. En segundo lugar, que el análisis de la microcirculación sigue siendo engorroso y conlleva mucho tiempo.
Por último, los dispositivos del futuro también deberían incluir monitorización metabólica permitiendo análisis de gases y mediciones de electrolitos en sangre. Así, utilizando un enfoque multimodal, los dispositivos del futuro no solo deberían ser fiables y menos invasivos.
También deberían ayudar a los clínicos a predecir los posibles eventos adversos y a ofrecer las terapias más adecuadas para poder contribuir a un abordaje más personalizado de los pacientes críticos.
¿Eres Anestesiólogo o Reanimador? Inscríbete ahora en el Itinerario Formativo ATI14
Artículo tomado de la lección del Itinerario Formativo ATI14 del Dra. Ana Pérez Carbonell : «Monitorización hemodinámica en el paciente crítico»
Si quieres información sobre nuestros cursos déjanos tus datos y te contactaremos








Debe estar conectado para enviar un comentario.